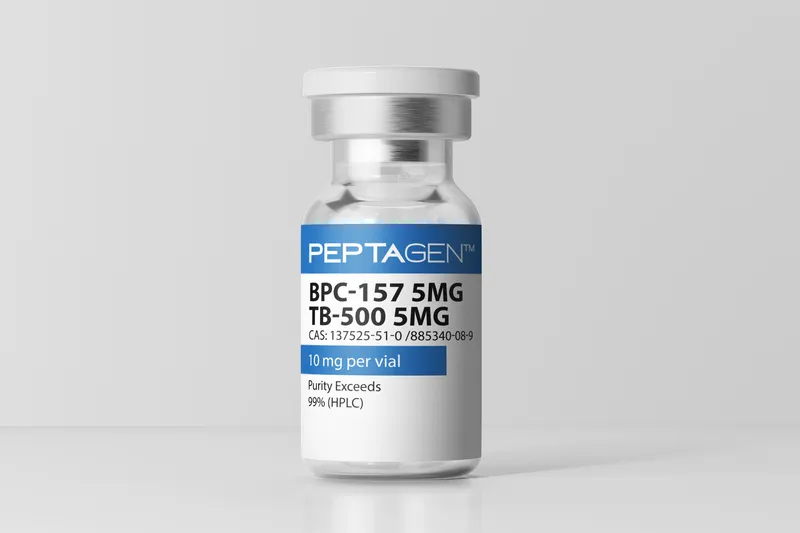
BPC-157 5mg
99,00 zł - 149,00 zł
Specyfikacje
- ilość mg: 5mg, 10mg
Tylko do badań
Ten produkt jest przeznaczony wyłącznie do celów badawczych i nie jest przeznaczony do spożycia przez ludzi.
BPC-157 – peptyd do badań naukowych (RUO)
Opis ogólny
BPC-157 to syntetyczny peptyd oferowany wyłącznie w klasie Research Use Only (RUO), przeznaczony do zastosowań badawczych w środowisku laboratoryjnym. Jest wykorzystywany w projektach z zakresu biologii molekularnej i biologii komórki, w których analizuje się odpowiedzi komórkowe na krótkie peptydy.
Charakterystyka naukowa
BPC-157 jest peptydem badawczym należącym do grupy krótkich sekwencji peptydowych stosowanych w modelach eksperymentalnych do analizy szlaków sygnalizacyjnych i regulacji procesów komórkowych. W badaniach in vitro może służyć do obserwacji zmian w ekspresji genów, aktywności wybranych białek sygnałowych oraz markerów odpowiedzi komórkowej. Związek bywa opisywany jako fragment białka pochodzenia żołądkowego (BPC), co jest wykorzystywane jako kontekst w pracach badawczych nad mechanizmami komórkowymi. Produkt w formie liofilizatu ułatwia przechowywanie zgodnie ze standardami laboratoryjnymi oraz kontrolę jakości w analizach chemicznych.
Zastosowanie badawcze
- Badania in vitro nad szlakami sygnalizacyjnymi i odpowiedzią komórkową na bodźce peptydowe.
- Analiza ekspresji genów oraz profili białkowych w modelach komórkowych (np. ścieżki stresu komórkowego).
- Projekty dotyczące interakcji peptyd–receptor i kaskad wtórnych przekaźników w układach badawczych.
- Zastosowanie jako materiał referencyjny w analizach biochemicznych i analitycznych (np. HPLC, LC‑MS).
- Badania stabilności krótkich peptydów oraz ich degradacji w warunkach laboratoryjnych.
Specyfikacja techniczna
- Forma: liofilizat
- Czystość: 99% (HPLC)
- Numer CAS: do uzupełnienia (wymaga potwierdzenia dla konkretnej postaci/soli oferowanej w produkcie)
- Ilość: 10 lub 5 mg na fiolkę
- Klasa produktu: Research Use Only (RUO)
- Opakowanie: szczelnie zamykana fiolka laboratoryjna przeznaczona do użytku badawczego
Informacje dodatkowe
Produkt przeznaczony jest wyłącznie dla wyspecjalizowanych laboratoriów oraz personelu przeszkolonego w pracy z odczynnikami peptydowymi. Przechowywanie i obsługa powinny odbywać się zgodnie ze standardowymi procedurami bezpieczeństwa i jakości obowiązującymi w laboratoriach.
⚠️ Research Use Only (RUO)
Produkt przeznaczony wyłącznie do badań naukowych i laboratoryjnych.
Nie jest przeznaczony do stosowania u ludzi ani zwierząt.
Nie stanowi leku, suplementu diety ani wyrobu medycznego.
Powiązane produkty
TB-500
N-acetyl Semax Amidate 10mg
DSIP 10mg